Архів ІІІ курс (34, 39 гр. ) 2022-2023н.р.
Дистанційне навчання з хімії
Шановні учні! В цьому блозі я буду проводити з вами дистанційне навчання. Зв'язок будемо підтримувати за допомогою вайбера.
Продовжуємо працювати за підручником П.Попель "Хімія",11кл., рівень стандарту, 2019
електронна версія :
https://pidruchnyk.com.ua/470-hmya-popel-kriklya-11-klas.html
Число для учнів 34 групи
22.03.23, 28.03.23 Тема програми. Хімія і прогрес людства.
Урок № 28,29. Тема.Роль хімії у розв'язанні продовольчої і сировинної проблем.
Опрацюйте параграф 34 с.210 підручника, перегляньте відео і запишіть в чому полягає роль хімії у розв'язанні продовольчої проблеми.
https://www.google.com/search?q=%D0%BF%D1%80%D0%B5%D0%B7%D0%B5%D0%BD%D1%82%D0%B0%D1%86%D1%96%D1%8F+%D1%80%D0%BE%D0%BB%D1%8C+%D1%85%D1%96%D0%BC%D1%96%D1%97+%D1%83+%D1%80%D0%BE%D0%B7%D0%B2%27%D1%8F%D0%B7%D0%B0%D0%BD%D0%BD%D1%96+%D0%BF%D1%80%D0%BE%D0%B4%D0%BE%D0%B2%D0%BE%D0%BB%D1%8C%D1%87%D0%BE%D1%97+%D0%BF%D1%80%D0%BE%D0%B1%D0%BB%D0%B5%D0%BC%D0%B8&oq=%D0%BF%D1%80&aqs=chrome.0.69i59l2j69i57j69i59j0i67j69i61l3.14635j0j7&sourceid=chrome&ie=UTF-8#fpstate=ive&vld=cid:086d2a89,vid:6f7vuwEc6NY
Число для учнів 34 групи Число для учнів 39 групи . 14.03.23, 21.03.23 .......
Тема програми. Хімія і прогрес людства.
Уроки № 26,27Тема. Роль хімії у
створені нових матеріалів, розвитку нових напрямів технологій.
Опрацюйте параграф 34 до статті "Хімія в рохв'язанні продовольчої проблеми" підручника.
Наведіть приклади металічних і неметалічних матеріалів, які
застосовуються для виробництва сільськогосподарських машин.
Число для учнів 34 групи Число для учнів 39 групи . 07.03.23 21.04.23 Тема програми. Неорганічні речовини і їхні властивості.
Урок № 25. Контрольна робота.
До 15.00 21.04.23 пройти тестування
https://naurok.com.ua/test/join?gamecode=5290638
Число для учнів 34 групи Число для учнів 39 групи . 28.02.23 21.04.23 Тема програми. Неорганічні речовини і їхні властивості.
Урок № 24. Узагальнення знань.
Повторіть матеріал && 14 - 27 і пройдіть тестування до 20.00 21.04 .23
https://naurok.com.ua/test/join?gamecode=8829662
Число для учнів 34 групи Число для учнів 39 групи . 2102.23 0902.23 Тема програми. Неорганічні речовини і їхні властивості.
Урок 23. Практична робота 1.
Тема. Генетичні зв’язки між неорганічними речовинами.
Ознайомтесь з інструцією, правилами техніки безпеки, запишіть тему, мету, генетичний ланцюг, посередині аркуша напишіть "Хід роботи", перегяньте відео спочатку першого досліду і опишіть його (дайте відповіді на запитання), потім перегляньте відео до кожного досліду і опишіть кожний дослід. У висновках записуйте, із яких речовин можна добути данну речовину.
Тема. Генетичні зв’язки між неорганічними речовинами
Мета: навчитися експериментально доводити наявність генетичного зв’язку між неорганічними речовинами на прикладі складеного фрагмента генетичного ланцюга
Обладнання: штатив із пробірками, піпетка, газовідвідна трубка, пальник (спиртівка)
Реактиви: мідний дріт,розчини: натрій гідроксиду, сульфатної кислоти, нітратної кислоти.
Завдання: складіть фрагмент генетичного ланцюга з речовин у наведених переліках. Перегляньте відео проведення дослідів і опишіть спостереження та складіть рівняння реакцій. Для реакцій йонного обміну складіть молекулярне та йонно-молекулярне рівняння. Оформіть звіт, давши відповіді на питання.
Генетичний ланцюг
Мідь → купрум (ІІ) оксид → купрум(ІІ) сульфат → купрум (ІІ) гідроксид→ купрум (ІІ) нітрат
Правила безпеки:
Перегляньте відео за посиланням https://youtu.be/BiuvThAaO18
Хід роботи
Перегляньте відео за посиланнями та запишіть спостереження і хімічні реакції до дослідів
Перелік 1 . Запишіть фрагмент генетичного ланцюга хімічними формулами
_Cu_ → _CuO__ → _CuSO4_ → _Cu(OH)2_ → _Cu(NO3)2_ .
Відповідно до даного генетичного ланцюга запишіть порядок виконання експерименту. (використовуйте посилання на відео досліди)
1)  Перегляньте відео фрагмент https://cutt.ly/NygjkiB та запишіть:
Перегляньте відео фрагмент https://cutt.ly/NygjkiB та запишіть:
порядок виконання експерименту (записати які дії потрібно виконати для першої ланки генетичного ланцюга) __________________________________________________________
__________________________________________________________
__________________________________________________________
Спостереження
- запишіть, яку ознаку реакції ви спостерігали під час досліду;
_____________________________________________________________
_________________________________________________________
- складіть рівняння реакцій. Для реакцій йонного обміну складіть молекулярне та йонно-молекулярне рівняння.
____________________________________________________________________________________________________________________________________________________________________________________________
Висновок:_______________________________________________________
________________________________________________________________

2) Перегляньте відео фрагмент https://cutt.ly/bygkYu0 та запишіть:
порядок виконання експерименту (записати які дії потрібно виконати для другої ланки генетичного ланцюга) __________________________________________________________
__________________________________________________________
__________________________________________________________
Спостереження
- запишіть, яку ознаку реакції ви спостерігали під час досліду;
_____________________________________________________________
_________________________________________________________
- складіть рівняння реакцій. Для реакцій йонного обміну складіть молекулярне та йонно-молекулярне рівняння.
____________________________________________________________________________________________________________________________________________________________________________________________
Висновок:_______________________________________________________
________________________________________________________________

3) Перегляньте відео фрагмент https://cutt.ly/AygluO8 та запишіть:
порядок виконання експерименту (записати які дії потрібно виконати для третьої ланки генетичного ланцюга) __________________________________________________________
__________________________________________________________
__________________________________________________________
Спостереження
- запишіть, яку ознаку реакції ви спостерігали під час досліду;
_____________________________________________________________
_________________________________________________________
- складіть рівняння реакцій. Для реакцій йонного обміну складіть молекулярне та йонно-молекулярне рівняння.
____________________________________________________________________________________________________________________________________________________________________________________________
Висновок:_______________________________________________________
________________________________________________________________
4)  Перегляньте відео фрагмент https://cutt.ly/wyglnJx та запишіть:
Перегляньте відео фрагмент https://cutt.ly/wyglnJx та запишіть:
порядок виконання експерименту (записати які дії потрібно виконати для четвертої ланки генетичного ланцюга) __________________________________________________________
__________________________________________________________
__________________________________________________________
Спостереження
- запишіть, яку ознаку реакції ви спостерігали під час досліду;
_____________________________________________________________
_________________________________________________________
- складіть рівняння реакцій. Для реакцій йонного обміну складіть молекулярне та йонно-молекулярне рівняння.
____________________________________________________________________________________________________________________________________________________________________________________________
Висновок:_______________________________________________________
______________________________
Число для учнів 34 групи Число для учнів 39 групи
07.02.23, 14.02.23 02.02.23, 09.02.23
Тема програми. Неорганічні речовини і їхні властивості.
Уроки№№ 21, 22. Тема. Генетичні зв'язки між основними класами неорганічних сполук.
Переглянути відео, опрацювати текст, виконати завдання із тексту
У підручнику цей матеріал викладено у параграфі 33 на с.198
1Виписати формули всіх:а) основ
б) кислот
в) оксидів
г)солей
Cu(OH)2 ,Na2O ,P2O5 , HNO3 , AL2(SO4)3, KOH ,HCI
Fe(OH)2, CaO , SO3 , H3PO4 , MgCI2, NaOH , H2S
Fe(OH)3 , K2O ,CO2 , HCI , Zn3(PO4)2, Ba(OH)2, HNO3.
Розглядаючи хімічні властивості сполук різних класів, можна простежити, як вони пов’язані за походженням, тобто скласти генетичні ряди, в яких простежується споріднений зв’язок між класами неорганічних сполук.
Генетичний зв’язок — це зв’язок між речовинами різних класів, що ґрунтується на взаємоперетворенні речовин і показує походження одних речовин від інших.
Знання генетичних зв’язків пояснює різноманітність класів неорганічних сполук і речовин у природі, відкриває перед ученими перспективи створення нових речовин.
Було давно помічено, що речовини, які беруть свій початок від простих речовин — металів, суттєво відрізняються за властивостями від речовин, що беруть початок від неметалів. Тому розрізняють два генетичних ряди: генетичний ряд металів та генетичний ряд неметалів.
Генетичний ряд металів. Генетичний ряд металів має такий
вигляд: ___
метал —> основний оксид —>основа (луг) —> сіль.
Метал, що започатковує генетичний ряд, наявний в усіх його складних речовинах, наприклад:
1 2 3
Ca —> CaO —>Са(ОН)2 —>СаС12
1) 2Са + 02 = 2СаО;
2) СаО + Н20 = Са(ОН)2;
3) Са(ОН)2 + 2НС1 = СаС12 + 2Н20.
Правило генетичних зв’язків:
1. Кількість стрілочок у схемі відповідає кількості рівнянь хімічних реакцій, які необхідно скласти.
2. Сполуки, записані перед стрілочкою, обов’язково мають вступити в хімічну реакцію.
3. Сполуки, записані пір ля стрілочки, мають утворитися внаслідок реакції.
Проте, як вам відомо, нерозчинну основу не можна добути з оксиду, піддавши його взаємодії з водою. Тому генетичний зв’язок ускладнюється на одну ланку:
метал —> основний оксид —>сіль —> основа —> інша сіль.
Для заліза та сполук Феруму він має вигляд:
1 2 3 4
Fe —> FeO—> FeS04 —> Fe(OH)2 —> FeCl2
1) 2Fe+O2=2FeO
2) FeO + H2SO4=FeSO4+H2O
3)  FeSO4+2NaOH =Fe(OH)2 +Na2SO4
FeSO4+2NaOH =Fe(OH)2 +Na2SO4
4) Fe(OH)2+2HCl= FeCl2+2H2O
Генетичний ряд неметалів. Генетичний ряд неметалів вибудовується за тим самим принципом, що й металів, лише гідрат оксиду в ньому не основа, а кислота:
неметал —> кислотний оксид —> кислота —> сіль.
Розглянемо генетичний ряд неметалів на прикладі сірки:
1 2 3
S —> S02 —> Н2S03 —> К2S03
1) S + 02 = S02;
2) Н20 + S02 = Н2S03;
3) 2КОН + Н2S0з = К2S03 + 2Н20.
2. Генетичний ряд неметалів, у якому основою виступає нерозчинна кислота. Цей ряд можна представити за допомогою таких перетворень:
неметал —> кислотний оксид —сіль —> кислота —> кислотний оксид —> неметал.
Наприклад, генетичний ряд Сіліцію:
1 2 3 4 5
Si —> SіO2 —> Na2SiО3 —> Н2 SіО3 —> SiO2 —> Si.
1) Si + O2 = SіO2
2) SіO2 + 2NaОH = Na2SiО3 + Н2 О
3) Na2SiО3 + 2НCl = 2NaCl + Н2SiО3
4) Н2SiО3 = SiО2 + Н2 О
5) SiО2 = Si + О2
Отже, ви ознайомилися з типовими варіантами генетичних рядів металів і неметалів.
Проте необов’язково, щоб з утворенням солі генетичний ряд завершувався. Його можна продовжити і, зокрема, у зворотному напрямі:
1 2 3 4 5 6 7
Cu —> CuO —> CuS04 —>Cu(OH)2 —> CuCl2 —> Cu(OH)2 —> CuO —> Cu
1) 2Cu + 02 = 2CuO;
2) CuO + H2S04 - CuS04 + H20;
3) CuS04 + 2KOH - Cu(OH)2 + K2S04;
4) Cu(OH)2 + 2HC1 - CuCl2 + 2H20.
5) CuСl2 + 2NaOH = Cu(OH)2 + NaCl
t
6) Си(ОН)2 —> CuO + Н20;
t
7) CuO + Н2 —> Cu + Н20.
Варіант I
Дано ряд речовин:
Са(NО3), Н2S04, Са(ОН)2, SiО2, Са, А1(0Н)2, Н8, СаО, РеS04, Р205
Випишіть речовини, що утворюють генетичний ряд; складіть схему цього зв’язку, напишіть рівняння реакцій, з допомогою яких можна його здійснити.
Варіант II
Дано ряд речовин:
КОН, S03, КNO3, НN03, K, К 20,Сu, Na 2So 4, Al(OH)3
Випишіть речовини, що утворюють генетичний ряд; складіть схему цього зв’язку, напишіть рівняння реакцій, з допомогою яких можна його здійснити
Число для учнів 34 групи Число для учнів 39 групи . 31.01.23 26.01.23, 0202.23 Тема програми. Неорганічні речовини і їхні властивості.
Уроки №19,20. Тема. Мінеральні добрива.Поняття про кислотні та лужні грунти.
1.Прочитайте §30 підручника.(с.180.)
2.Дайте визначення мінеральних добрив (письмово)
3.Складіть схему класифікації добрив (письмово)
4. Дайте відповіді на запитання: які грунти називаються кислими,
а які- лужними? ( письмово)
5.Робота з підручником: виконайте завдання №240, №241,№243 на с. 186.
6. До 03.02.23 до 20.00 пройти тестування
Число для учнів 34 групи Число для учнів 39 групи ...... 26.01.23 Тема програми. Неорганічні речовини і їхні властивості.
Урок№ 18. Тема. Біологічне значення металічних і неметалічних елементів.
Опрацюйте # 32 с.194 підручника,перегляньте відео
https://www.youtube.com/watch?v=cagln8lYOpE
1.Випишіть елементи-органогени.
2.Як до організмів рослин потрапляють елементи С, Н, О?
3. ............................................................................N, S, P?
4.Яких елементів металічних чи неметалічних більше в організмах тварин?
5.Виконайте завдання для допитливих із блогу.
Число для учнів 34 групи Число для учнів 39групи 08.11.23 19.01.23
Тема програми. Неорганічні речовини і їхні властивості.
Урок № 17. Тема. Сучасні силікатні матеріали.
Прочитайте текст і запишіть:
1.Назви сучасних силікатних матеріали.
2.Сировина для виробництва скла: склад, формула.
3.Які споруди використовуються для виготовлення скла?
4.За якої t варять скло?
5.Галузі застосування склониток.
6.Сировина для виготовлення цементу.
7.Склад бетону.
8.Перелічити керамічні виоби.
Цемент, бетон, цегла, кераміка, скло — продукція силікатної промисловості.
СКЛО
Виготовлення скляних виробів можливе лише з гарячої розплавленої маси, а розм'якшуватися скло починає за температури 900 °С, рідким скло стає за температури 1500 °С.Виготовляють (варять) звичайне віконне скло із соди Na2CO3, вапняку CaCO3 та кварцового піску SiO2 за температури 1500 °С у спеціальних печах безперервної дії. За добу з однієї печі одержують до 300 т продукції. Про розміри такої печі, свідчить її варильний басейн довжиною у 40 м, шириною у 10 м і висотою у 1,5 м.
Хімізм виготовлення скла ґрунтується на властивостях карбонатів розкладатися під час нагрівання та властивостях основних і кислотних оксидів взаємодіяти між собою:
CaCO3= СаО + CO2↑;
СаО + SiO2 = CaSiO3;
Na2CO3 + SiO2= Na2SiO3 + CO2↑;
CaCO3 + SiO2 = CaSiO3 + CO2↑.
Сировину беруть у співвідношенні, що забезпечує утворення скла з приблизно таким складом: Na2O · CaO · 6SiO2.
Скло звичайне (з нього виготовляють віконні шибки, скляні банки і пляшки) — прозорий аморфний сплав суміші натрій силікату з кальцій силікатом і кварцовим піском.
Здатність скла пропускати сонячні промені, поступовий перехід із твердого стану в рідкий через відсутність постійної точки плавлення й кипіння, стійкість до дії кислот, лугів тощо, а також урізноманітнення інших його фізичних характеристик за рахунок уведення добавок дають змогу одержувати різні види скла, що широко використовуються.
Заміною одних компонентів сировини на інші, уведенням різноманітних добавок, зміною вмісту окремих складових скла виготовляють різні його види.
РІЗНОВИДИ СКЛА ТА ЇХ ЗАСТОСУВАННЯ. Якщо натрій карбонат замінити на калій карбонат, то утвориться скло, міцніше за віконне. З нього виготовляють хімічний посуд, у якому можна кип'ятити рідини, не боячись, що посуд трісне.

Мал. 79. Предмети, виготовлені з різних видів скла
Якщо чистий кварцовий пісок розплавити, а потім дати йому повільно охолонути, то утвориться кварцове скло. Лабораторний посуд, виготовлений з такого скла, можна розжарити до білого кольору, після чого опустити в холодну воду, і він не трісне. Кварцове скло пропускає ультрафіолетові промені, цю його властивість використовують у медицині (кварцові лампи), соляріях.
Установлено, що ферум(ІІІ) оксид надає склу коричневого кольору, кобальт(ІІ) оксид робить скло синім, хром(ІІІ) оксид — зеленим. Від додавання невеликої кількості порошку золота скло стає рубіновим, тобто пурпурово-червоним.
Одним із досягнень хімічної науки ХХ ст. стало створення склониток і скловолокна (мал. 80). Відтепер склонитки використовують як світловоди для передавання зображень і звуків. Без цього не існувало б кабельного телебачення, телефонного зв'язку, не було б приладів, що діагностують стан внутрішніх органів людини.

Мал. 80. Скловолокно
Кришталеве скло виготовляють з калій карбонату, плюмбум(ІІ) оксиду, уміст якого дорівнює майже 24 %, і кварцового піску. Це скло має високий коефіцієнт заломлення світла, тому його використовують в оптиці (виготовлення лінз і призм). Оскільки кришталеве скло має яскравий блиск, його гранують, щоб виготовити красиві вази й столовий посуд.
Емальований посуд вам добре відомий. Емаль — це матеріал, виготовлений із звичайної скломаси шляхом додавання до неї станум(IV) оксиду. Кольоровою емаллю оздоблюють прикраси (мал. 81, а), картини (мал. 81, б), вази (мал. 81, в) тощо.

Мал. 81. Оздоблення емаллю
За певних умов аморфну скломасу піддають частковій перекристалізації з утворенням білого, непрозорого, термостійкого й міцного матеріалу, що називається ситал.
З нього виготовляють побутовий вогнетривкий кухонний посуд: каструлі, форми для запікання, жаровні, сковорідки тощо (мал. 82).

Мал. 82. Вогнетривкий кухонний посуд із ситалу
ЦЕМЕНТ. Споруди високої міцності й тривалого призначення (будинки, тунелі, мости) будують з обов'язковим використанням цементу (за винятком дерев'яних будиночків і невеликих містків місцевого значення). Цей матеріал має рідкісну властивість — з роками його твердість збільшується.
Є різні сорти цементу, серед найуживаніших — портландцемент. Як сировину для виробництва цементу використовують вапняк і глину, рідше мергель — природну суміш цих двох речовин. Формулу вапняку ви знаєте, склад глини передають записом Al2O3 · 2SiO2 · 2Н2О.
Якщо передати склад цементу формулами оксидів, то виявиться, що він містить 62-76 % СаО, 20-24 % SiO2, 4-7 % Al2O3, незначну кількість Fe2O3 та MgO.
На будівництві цемент змішують з піском і водою. Утворену суміш називають цементним або будівельним розчином, з часом він стає кам'янистим. Цементний розчин є незамінним зв'язувальним матеріалом для цегли, будівельних блоків тощо. Затвердіння відбувається внаслідок того, що складові речовини цементу з водою утворюють відповідні кристалогідрати. Давній Київ наші предки будували з використанням в'яжучої маси на зразок цементу, яку виготовляли з вапняку і випаленої глини «цем'янки». Перші цементні заводи України були збудовані на Донеччині і Рівненщині наприкінці ХІХ ст. Архітектор В. Городецький в 1903 р. використав вітчизняний цемент для виготовлення оздоблення однієї з найкрасивіших будівель ХХ ст., яка й донині прикрашає Київ (мал. 83).

Мал. 83. Будинок з химерами архітектора В. Городецького
Суміш щебеню (подрібненої гірської породи гранітного походження), піску і цементу називається бетон, без якого неможливе зведення мостів, будинків, гребель. Бетон, підсилений залізним каркасом, називається залізобетоном.
Силікатна промисловість включає також керамічне виробництво. До керамічних виробів належать будівельна цегла (мал. 84, а) (її виробляють найбільше), кахлі, облицювальні плитки, раковини умивальників, посуд із порцеляни і фаянсу тощо (мал. 84, б).

Мал. 84. Вироби з кераміки
Особливістю керамічного виробництва є те, що вироби після формування випалюють. З однорідної суміші глини, піску і води формують цеглини, а потім їх висушують у призначених для цього печах. Глина, змочена водою, стає схожою на пластилін і їй можна надати різної форми. На цій властивості глини ґрунтується гончарство. Амфори, глечики, миски — ці та інші гончарні вироби знаходять археологи під час розкопок давніх поселень . І нині, незважаючи на велику різноманітність матеріалів, люди не відмовилися від створення гончарних виробів . Україна славиться такими виробами, їх виробництвом займаються гончарі в різних регіонах. Одним з найбільших осередків виробництва гончарної кераміки в Україні є селище міського типу Опішня Полтавської області. Для виготовлення порцеляни використовують білу глину каолін Al2O3 · 2SiO2 · 2H2O, у меншій кількості беруть польовий шпат K2O · Al2O3 · 6SiO2 і кварцовий пісок SiO2. У техніці застосовують електроізоляційні властивості порцеляни, її хімічну стійкість. З менш очищеної сировини, ніж та, з якої виробляють порцеляну, одержують грубіший матеріал — фаянс, що використовують так само, як порцеляну.
Тема програми. Неорганічні речовини і їхні властивості.
Число для учнів 39 групи 22.12.22, 19.01.23
Уроки №15, 16 Тема. Поняття про жорсткість води.
Опрацюйте & 28 і запишіть відповіді на запитання:
1.Чим зумовлена твердість води?
2.Види тведості води.
3.Чим зумовлена тимчасова твердість води? Як її усунути?
4.Чим зумовлена постійна твердість води? Як її усунути?
5.Яка негативна дія твердої води на виробництві і в побуті?
7.Підготуйте проєкт № 20.Усунення тимчасової і постійної жорсткості води.
34групи Число для учнів 39 групи 29.12.22
Число для учнів
Тема програми. Неорганічні речовини і їхні властивості.
Урок № 14. Контрольна робота.
До 12.00 29.12.22 пройти тестування.
34групи Число для учнів 39 групи 15.12.22
Число для учнів
01.11.22 Тема програми. Неорганічні речовини і їхні властивості.
Урок № 13. Практична робота№1
Тема. Дослідження якісного складу солей.
Мета: навчитись досліджувати якісний склад солей
Перегляньте презентацію, запишіть:
Урок № 13. Практична робота№1
Тема. Дослідження якісного складу солей.
Мета: навчитись досліджувати якісний склад солей
Число для учнів 34групи Число для учнів 39 групи
01.11.22 Тема програми. Неорганічні речовини і їхні властивості. ......
Урок № 12. Тема. Якісні реакції на деякі йони.
1. Переглянути презентацію і виппсати якісні реагенти на наведені аніони і катіони.
2. Підготувати проєкт №19 "Властивості і застосування карбонатів, нітратів і ортофосфатів лужних і лужноземельних металічних елементів, солей амонію."
(презентація, реферат, .....)
Число для учнів 39 групи 08.12.22
Тема програми. Неорганічні речовини і їхні властивості.
Урок№11. Узагальнення знань.
До21.00 10.12.22 пройти тестування
https://naurok.com.ua/test/join?gamecode=3841940
Число для учнів 39 групи 01.12.22
Тема програми. Неорганічні речовини і їхні властивості.
Урок №10. Тема. Солі.
1. Опрацюйте & 27, перегляньте відео, оформіть лабораторні досліди №7, № 8.
Зразок оформлення дослідів див. в уроку №9
Лабораторний дослід № 7. ( с. 191 )
Тема. Виявлення у розчинах силікат - іонів.
https://www.youtube.com/watch?v=lrQhqecOxlA
Лабораторний дослід №8(с._192)
Тема. Виявлення у розчинах ортофосфат-іонів.
https://www.youtube.com/watch?v=gwYMOOgEQns
2. Переглянути презентацію і виписати якісні реагенти на наведені аніони і катіони.
Число для учнів 34групи Число для учнів 39 групи
Тема програми. Неорганічні речовини і їхні властивості. 15.11.22
Урок № 9. Тема. Солі.
Прочитайте цей матеріал, пригадайте як складаються формули солей, як дають назви солям.
Потім вивчіть & 27 с.163 підручника, перегляньте відео і оформіть лабораторні досліди №№ 3-6 на с.189.
завдання№2https://www.youtube.com/watch?v=SXXtiKSSRpM
завдання №3 https://www.youtube.com/watch?v=mdL-8mVTU70
Зразок оформленння лаб. досліду:
Лабораторний дослід № 3.
Тема. Виявлення в розчині катіонів барію.
Взяли: розчин барій нітрату
Додали: розчин сульфатної кислоти
Спостерігали: утворення білого осаду
Висновок: записати рівняння реакції між барій нітратом та сульфатною кислотою (молекулярне та йоннні)
Йони Барію можна виявити за допомогою речовин,що містять сульфат-іони. При додаванні до розчину,що містить йони Барію сульфатної кислоти або її солей утворюється білий осад.
Солями називають продукти заміщення атомами металічних елементів атомів Гідрогену у молекулах кислот.
Солі — складні речовини, що складаються з металічних елементів і кислотних залишків.
При складанні назв солей дотримуються наступної схеми:
назва металічного елемента у називному відмінку + назва кислотного залишку: кальцій сульфат, натрій нітрат, алюміній ортофосфат, тощо.
Те, який суфікс застосовують у назві солі, залежить від цілого ряду чинників, а саме:
1) якщо до складу солі входить кислотний залишок безоксигенової кислоти (наприклад, хлоридної, (соляної) HCl), тоді використовується суфікс –ид (наприклад, хлорид);
2) якщо до складу солі входить кислотний залишок кислоти, в назві якої є закінчення –а (наприклад, сульфатна H2SO4), у назві солі використовується суфікс –ат (наприклад, сульфат);
3) якщо до складу солі входить кислотний залишок кислоти, в назві якої є суфікс –ист (наприклад, сірчиста H2SO3) , у назві солі використовується суфікс –іт (наприклад, сульфіт).
Якщо до складу солі входить металічний елемент, що має змінну валентність, то його валентність у даній сполуці вказують римськими цифрами в дужках одразу (без пробілу) після назви металу.
Існують солі, до складу яких замість металічного хімічного елемента входить одновалентна група амонію
NH4I (йон амонію
NH4+ ).
Зверни увагу!
При складанні формул солей дотримуються правила: сума валентностей металічного хімічного елемента повинна дорівнювати сумі валентностей кислотного залишку.
Тема програми. Неорганічні речовини і їхні властивості.
Урок № 8. Тема.Натрій гідроксид, кальцій гідроксид.
Опрацювати & 26, законспектувати с.161
Дата проведення для учнів 39 групи
Тема програми. Неорганічні речовини і їхні властивості. 08.11.22
Урок №7. Тема. Основи.
Прочитати текст, законспектувати, пройти тестування до 09.11.22 до 08.00
https://naurok.com.ua/test/join?gamecode=6382370
В підручнику цей матеріал викладено у &26 c/158 до статті " Застосування гідроксидів ..." на с.161.
Основами називають складні речовини, до складу яких входять металічні хімічні елементи, сполучені з "днією або декількома гідроксогрупами (групами атомів —OH).
Виходячи з цього, загальну хімічну формулу основ можна зобразити наступним чином:
M(OH)n,
де M — знак металічного хімічного елемента,
а n — індекс, чисельно співпадаючий з валентністю металу.
Зверни увагу!
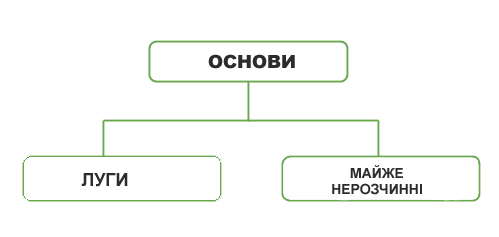
Основи класифікують за двома ознаками — розчинністю у воді, і кількістю гідроксильних груп.
Розчинні у воді основи називають лугами.
За їх здатністю розчинятися у воді основи ділять на розчинні і практично нерозчинні:
Кислотність основ
За числом гідроксильних груп основи буваоть однокислотні (NaOH, KOH, LiOH), двокислотні ( Ca(OH)2, Fe(OH)2, Cu(OH)2), багатокислотні (Fe(OH)3).
Загальні хімічні властивості лугів
Фактично індикатор реагує на наявність гідроксидних груп, що містяться в розчині будь якого лугу. При цьому протікає хімічна реакція з утворенням нового продукту, ознакою протікання якої є зміна забарвлення речовини.
Зміна забарвлення індикаторів у розчинах лугів
Індикатор | Зміна забарвлення індикатора |
| Лакмус | Фіолетовий лакмус стає синім |
| Фенолфталеїн | Безбарвний фенолфталеїн стає малиновим |
Універсальний
індикатор | Універсальний індикатор стає синім |
2. Луги взаємодіють з кислотами, утворюючи сіль і воду.
Реакції обміну між лугами і кислотами називають реакціями нейтралізації.
Наприклад, при взаємодії натрій гідроксиду з нітратною кислотою утворюється натрій нітрат і вода:
NaOH+HNO3=NaNO3+H2O.
3. Луги взаємодіють з кислотними оксидами, утворюючи сіль і воду.
Наприклад, при взаємодії кальцій гідроксиду з карбон(IV) оксидом (вуглекислим газом), утворюється кальцій карбонат і вода:
Ca(OH)2+CO2=CaCO3⏐↓+H2O.
4. Луги можуть взаємодіяти з розчинними у воді солями.
Зверни увагу!
Реакція обміну між основою і сіллю можлива лише у тому випадку, якщо обидві вихідні речовини є розчинними у воді, а в результаті реакції утворюється хоча б одна нерозчинна речовина (випадає осад).
Наприклад, при взаємодії калій гідроксиду з купрум(II) сульфатом утворюється калій сульфат і купрум(II) гідроксид, який випадає в осад:
2KOH+CuSO4=K2SO4+Cu(OH)2⏐↓.
При взаємодії кальцій гідроксиду з натрій карбонатом утворюється кальцій карбонат (осад) і натрій гідроксид:
Ca(OH)2+Na2CO3=CaCO3⏐↓+2NaOH.
5. Малорозчинні луги при нагріванні розкладаються на оксид металу і воду.
Наприклад, якщо нагріти кальцій гідроксид, утворюється кальцій оксид і водяна пара:
Ca(OH)2=t°CaO+H2O↑⏐⏐.
Загальні хімічні властивості нерозчинних основ
1. Нерозчинні основи взаємодіють з кислотами, утворюючи сіль і воду.
Наприклад, при взаємодії купрум(II) гідроксиду з сульфатною кислотою утворюється купрум(II) сульфат і вода:
Cu(OH)2+H2SO4=CuSO4+2H2O.
2. Деякі нерозчинні основи можуть взаємодіяти з деякими кислотними оксидами, утворюючи сіль і воду.
Наприклад, при взаємодії купрум(II) гідроксиду з сульфур(IV) оксидом утворюється купрум(II) сульфіт і вода:
Cu(OH)2+SO2=t°CuSO3+H2O
3. Нерозчинні основи при нагріванні розкладаються на оксид металу і воду.
Наприклад, ферум(III) гідроксид при нагріванні розкладається на ферум(III) оксид і воду:
Число для учнів 34групи Число для учнів 39 групи 01.11.22
2Fe(OH)3=t°Fe2O3+3H2O. Тема програми. Неорганічні речовини і їхні властивості.
Урок №6. Тема. Застосування металів та їхніх сплавів.
1.Опрацювати статтю параграфа 23 с.136 . Виписати склад сплавів: чавун, нержавіюча сталь, бронза, латунь.
2.Написати які сплави використовують для виготовлення кухонного посуду.
Тема програми. Неорганічні речовини і їхні властивості.
Урок № 5 . Тема. Залізо: фізичні та хімічні властивості.
Опрацювати # 25 підручника, переглянути презентацію, https://naurok.com.ua/prezentaciya-na-temu-zalizo-fizichni-ta-himichni-vlastivosti-150828.html
І. виписати
1) електронну формулу феруму
2)хімічні властивості заліза (реакції заліза з неметалами, водою, кислотами, солями)
3) формули оксидів феруму , гідроксидів феруму,
4) їхні хімічні властивості
5) назви і формули залізних руд. Де вони використовуються? ІІ. Виконати вправу №195 а) і б).
Тема програми. Неорганічні речовини і їхні властивості.
Урок №4 Тема. Алюміній.
1) Вивчіть #24 підручника, перегляньте презентацію
https://naurok.com.ua/prezentaciya-po-temi-alyuminiy-fizichni-ta-himichni-vlastivosti-152646.html
запишіть фізичні та хімічні властивості алюмінію
2) Розв'яжіть задачу.
Сплав міді й алюмінію масою 15г обробили надлишком хлоридної кислоти й добули водень об'ємом 13,44л (н.у.).Обчисліть масові частки металів у сплаві.
Тема програми. Неорганічні речовини і їхні властивості.
Урок №3. Тема.Фізичні властивості металів.
Опрацюйте #23 статтю "Фізичні властивості" і запишіть фіз. властивості металів.
Які метали мають найвищу електропровідність?
Який метал найтвердіший?
Що значить феромагнетики?
Які метали є феромагнетиками?
До 20.00 28.09.22 пройти тестування
https://naurok.com.ua/test/join?gamecode=1769368
Тема програми. Неорганічні речовини і їхні властивості.
Урок№2.Загальна характеристика металів. Застосування металів та їхніх сплавів.
1) Вивчіть матеріал # 23 підручника до с. 135, до статті "Фізичні властивості"та перегляньте презентацію дайте письмові відповіді на запитання:
https://naurok.com.ua/prezentaciya-zagalna-harakteristika-metaliv-fizichni-ta-himichni-vlastivosti-metaliv-207453.html
1. Яких елементів у природі більше метал. чи неметал.?
2.Який метал у природі найпоширеніший?
3.Де у періодичній системі розміщені метали?
4. Яка кількість електронів перебуває на зовнішньому рівні атомів металів?
5.Атоми металів здатні втрачати чи приєднувати електрони?
6. Чи перетворюються атоми металів на катіони під час віддачі електронів?
(катіони - це позитивно заряджені йони. Йон - заряджена частинка.
аніон - негативно заряджена частинка)
7. Який хімічний зв'язок у металах?
8. Які кристалічні гратки у металах ?
2.Опрацювати статтю параграфа 23 с.136 . Виписати склад сплавів: чавун, нержавіюча сталь, бронза, латунь.